Водород — характеристика, физические и химические свойства. Водород
Характеристика s-элементов
К блоку s-элементов относятся 13 элементов, общим для которых является застраивание в их атомах s-подуровня внешнего энергетического уровня.
Хотя водород и гелий относятся к s-элементам из-за специфики их свойств их следует рассматривать отдельно. Водород, натрий, калий, магний, кальций - жизненно необходимые элементы.
Соединения s-элементов проявляют общие закономерности в свойствах, что объясняется сходством электронного строения их атомов. Все внешние электроны являются валентными и принимают участие в образовании химических связей. Поэтому максимальная степень окисления этих элементов в соединениях равна числу электронов во внешнем слое и соответственно равна номеру группы, в которой и находится данный элемент. Степень окисления металлов s-элементов всегда положительна. Другая особенность заключается в том, что после отделения электронов внешнего слоя остается ион, имеющий оболочку благородного газа. При увеличении порядкового номера элемента, атомного радиуса, уменьшается энергии ионизации (от 5,39 эВ y Li до 3,83 эВ y Fr), а восстановительная активность элементов возрастает.
Подавляющее большинство соединений s-элементов бесцветно (в отличие от соединений d-элементов), так как исключен обуславливающий окраску переход d-электронов с низких энергетических уровней на более высокие энергетические уровни.
Соединения элементов групп IA - IIA - типичные соли, в водном растворе они практически полностью диссоциируют на ионы, не подверженны гидролизу по катиону (кроме солей Be 2+ и Mg 2+).
водород гидрид ионный ковалентный
Для ионов s-элементов комплексообразование не характерно. Кристаллические комплексы s - элементов с лигандами H 2 O-кристаллогидраты, известны с глубокой древности, например: Na 2 В 4 O 7 10H 2 O-бура, KАl (SO 4) 2 12H 2 O-квасцы. Молекулы воды в кристаллогидратах группируются вокруг катиона, но иногда полностью окружают и анион. Вследствие малого заряда иона и большого радиуса иона щелочные металлы наименее склонны к образованию комплексов, в том числе и аквакомплексов. В качестве комплексообразователей в комплексных соединениях невысокой устойчивости выступают ионы лития, бериллия, магния.
Водород. Химические свойства водорода
Водород - наиболее легкий s-элемент. Его электронная конфигурация в основном состоянии 1S 1 . Атом водорода состоит из одного протона и одного электрона. Особенность водорода состоит в том, что его валентный электрон находится непосредственно в сфере действия атомного ядра. У водорода нет промежуточного электронного слоя, поэтому водород нельзя считать электронным аналогом щелочных металлов.
Как и щелочные металлы водород является восстановителем, проявляет степень окисления +1, Спектры водорода сходны со спектрами щелочных металлов. Со щелочными металлами сближает водород его способность давать в растворах гидратированный положительно заряженный ион Н + .
Подобно галогеном атому водорода не достает одного электрона. Этим и обусловлено существование гидрид-иона Н - .
Кроме того, как и атомы галогенов атомы водорода характеризуются высоким значением энергии ионизации (1312 кдж/моль). Таким образом, водород занимает особое положение в Периодической системе элементов.
Водород - самый распространенный элемент во вселенной: он составляет до половины массы солнца и большинства звезд.
На солнце и других планетах водород находится в атомарном состоянии, в межзвездной среде в виде частично ионизированных двухатомных молекул.
Водород имеет три изотопа; протий 1 Н, дейтерий 2 Д и тритий 3 Т, причем тритий - радиоактивный изотоп.
Молекулы водорода отличаются большой прочностью и малой поляризуемостью, незначительными размерами и малой массой и обладают большой подвижностью. Поэтому у водорода очень низкие температуры плавления (-259,2 о С) и кипения (-252,8 о С). Из-за высокой энергии диссоциации (436 кдж/моль) распад молекул на атомы происходит при температурах выше 2000 о С. Водород бесцветный газ без запаха и вкуса. Он имеет малую плотность - 8,99·10 -5 г/см При очень высоких давлениях водород переходит в металлическое состояние. Считается, что на дальних планетах солнечной системы - Юпитере и Сатурне водород находится в металлическом состоянии. Существует предположение, что в состав земного ядра также входит металлический водород, где он находится при сверхвысоком давлении, создаваемым земной мантией.
Химические свойства. При комнатной температуре молекулярный водород реагирует лишь со фтором, при облучении светом - с хлором и бромом, при нагревании с О 2 ,S, Se, N 2 , C, I 2 .
Реакции водорода с кислородом и галогенами протекают по радикальному механизму.
Взаимодействие с хлором - пример неразветвленной реакции при облучении светом (фотохимическая активация), при нагревании (термическая активация).
Сl+ H 2 = HCl + H (развитие цепи)
H+ Сl 2 = HCl + Сl
Взрыв гремучего газа - водородокислородной смеси - пример разветвленного цепного процесса, когда инициированние цепи включает не одну, а несколько стадий:
Н 2 + О 2 = 2ОН
Н+ О 2 = ОН+О
О+ Н 2 = ОН+ Н
ОН+ Н 2 = Н 2 О + Н
Взрывного процесса удается избежать, если работать с чистым водородом.
Поскольку для водорода характерна - положительная (+1) и отрицательная (-1) степень окисления, водород может проявлять и восстановительные, и окислительные свойства.
Восстановительные свойства водорода проявляются при взаимодействии с неметаллами:
Н 2 (г) + Cl 2 (г) = 2НCl (г),
2Н 2 (г) + О 2 (г) = 2Н 2 О (г),
Эти реакции протекают с выделением большого количества теплоты, что свидетельствуют о высокой энергии (прочности) связей Н-Сl, Н-О. Поэтому водород проявляет восстановительные свойства по отношению ко многим оксидам, галогенидам, например:
На этом основано применение водорода в качестве восстановителя для получения простых веществ из оксидов галогенидов.
Еще более сильным восстановителем является атомарный водород. Он образуется из молекулярного в электронном разряде в условиях низкого давления.
Высокой восстановительной активностью обладает водород в момент выделения при взаимодействии металла с кислотой. Такой водород восстанавливает CrCl 3 в CrCl 2:
2CrCl 3 + 2HСl + 2Zn = 2CrCl 2 + 2ZnCl 2 +H 2 ^
Важное значение имеет взаимодействие водорода с оксидом азота (II):
2NO + 2H 2 = N 2 + H 2 O
Используемое в очистительных системах при производстве азотной кислоты.
В качестве окислителя водород взаимодействует с активными металлами:
В данном случае водород ведет себя как галоген, образуя аналогичные галогенидам гидриды .
Гидриды s-элементов I группы имеют ионную структуру типа NaCl. В химическом отношении ионные гидриды ведут себя как основные соединения.
К ковалентным относятся гидриды менее электроотрицательных, чем сам водород неметаллических элементов, например, гидриды состава SiH 4 , ВН 3 , СН 4 . По химической природе гидриды неметаллов являются кислотными соединениями.
Характерной особенностью гидролиза гидридов является выделение водорода, реакция протекает по окислительно-восстановительному механизму.
Основной гидрид
Кислотный гидрид
За счет выделения водорода гидролиз протекает полностью и необратимо (?Н<0, ?S>0). При этом основные гидриды образуют щелочь, а кислотные кислоту.
Стандартный потенциал системы В. Следовательно, ион Н - сильный восстановитель.
В лаборатории водород получают взаимодействием цинка с 20% -й серной кислотой в аппарате Киппа.
Технический цинк часто содержит небольшие примеси мышьяка и сурьмы, которые восстанавливаются водородом в момент выделения до ядовитых газов: арсина SbH 3 и стабина SbH Таким водородом можно отравиться. С химически чистым цинком реакция протекает медленно из-за перенапряжения и хорошего тока водорода получить не удается. Скорость этой реакции увеличивается путем добавления кристалликов медного купороса, реакция ускоряется за счет образования гальванической пары Cu-Zn.
Более чистый водород образуется при действии щелочи на кремний или алюминий при нагревании:
В промышленности чистый водород получают электролизом воды, содержащей электролиты (Na 2 SO 4 , Ba (OH) 2).
Большое количество водорода образуется в качестве побочного продукта при электролизе водного раствора хлорида натрия с диафрагмой, разделяющей катодное и анодное пространство,
Наибольшее количество водорода получают газификацией твердого топлива (антрацита) перегретым водяным паром:
Либо конверсией природного газа (метана) перегретым водяным паром:
Образующаяся смесь (синтез-газ) используется в производстве многих органических соединений. Выход водорода можно увеличить, пропуская синтез-газ над катализатором, при этом СО превращается вСО 2 .
Применение. Большое количество водорода расходуется на синтез аммиака. На получение хлороводорода и соляной кислоты, для гидрогенизации растительных жиров, для восстановления металлов (Mо, W, Fe) из оксидов. Водород-кислородное пламя используют для сварки, резки и плавления металлов.
Жидкий водород используют в качестве ракетного топлива. Водородное топливо является экологически безопасным и более энергоемким, чем бензин, поэтому в будущем оно может заменить нефтепродукты. Уже сейчас в мире на водороде работает несколько сот автомобилей. Проблемы водородной энергетики связаны с хранением и транспортировкой водорода. Водород храня в подземных танкерах в жидком состоянии под давлением 100 атм. Перевозка больших количеств жидкого водорода представляет серьезную опасность.
10.1.Водород
Название "водород"относится и к химическому элементу, и к простому веществу. Элемент водород состоит из атомов водорода. Простое вещество водород состоит из молекул водорода.
а) Химический элемент водород
В естественном ряду элементов порядковый номер водорода – 1. В системе элементов водород находится в первом периоде в IA или VIIA группе.
Водород – один из самых распространенных элементов на Земле. Молярная доля атомов водорода в атмосфере, гидросфере и литосфере Земли (все вместе это называется земной корой) равна 0,17. Он входит в состав воды, многих минералов, нефти, природного газа, растений и животных. В теле человека в среднем содержится около 7 килограммов водорода.
Существуют три изотопа водорода:
а) легкий водород – протий
,
б) тяжелый водород – дейтерий
(D),
в) сверхтяжелый водород – тритий
(Т).
Тритий неустойчивый (радиоактивный) изотоп, поэтому в природе он практически не встречается. Дейтерий устойчив, но его очень мало: w D = 0,015% (от массы всего земного водорода). Поэтому атомная масса водорода очень мало отличается от 1 Дн (1,00794 Дн).
б) Атом водорода
Из предыдущих разделов курса химии вам уже известны следующие характеристики атома водорода:
Валентные возможности атома водорода
определяются наличием одного электрона на
единственной валентной орбитали. Большая
энергия ионизации делает атом водорода не
склонным к отдаче электрона, а не слишком высокая
энергия сродства к электрону приводит к
незначительной склонности его принимать.
Следовательно, в химических системах
образование катиона Н
невозможно, а соединения с анионом Н не очень устойчивы.
Таким образом, для атома водорода наиболее
характерно образование с другими атомами
ковалентной связи за счет своего одного
неспаренного электрона. И в случае образования
аниона, и в случае образования ковалентной связи
атом водорода одновалентен.
В простом веществе степень окисления атомов
водорода равна нулю, в большинстве соединений
водород проявляет степень окисления +I, и только в
гидридах наименее электроотрицательных
элементов у водорода степень окисления –I.
Сведения о валентных возможностях атома
водорода приведены в таблице 28. Валентное
состояние атома водорода, связанного одной
ковалентной связью с каким-либо атомом, в таблице
обозначено символом "H-".
Таблица 28. Валентные возможности атома водорода
Валентное состояние |
Примеры химических веществ |
|||
I |
HCl, H 2 O, H 2 S, NH 3 ,
CH 4 , C 2 H 6 , NH 4 Cl, H 2 SO 4 ,
NaHCO 3 , KOH |
|||
NaH, KH, CaH 2 , BaH 2 |
в) Молекула водорода
Двухатомная молекула водорода Н 2 образуется при связывании атомов водорода единственной возможной для них ковалентной связью. Связь образуется по обменному механизму. По способу перекрывания электронных облаков это s-связь (рис. 10.1 а ). Так как атомы одинаковы, связь неполярная.

Межатомное расстояние (точнее
равновесное межатомное расстояние, ведь атомы-то
колеблются) в молекуле водорода r
(H–H) = 0,74 A
(рис.10.1 в
), что значительно меньше суммы
орбитальных радиусов (1,06 A). Следовательно,
электронные облака связываемых атомов
перекрываются глубоко (рис. 10.1 б
), и связь в
молекуле водорода прочная. Об этом же говорит и
довольно большое значение энергии связи
(454 кДж/моль).
Если охарактеризовать форму молекулы граничной
поверхностью (аналогичной граничной поверхности
электронного облака), то можно сказать, что
молекула водорода имеет форму слегка
деформированного (вытянутого) шара (рис. 10.1 г
).
г) Водород (вещество)
При обычных условиях водород – газ без
цвета и запаха. В небольших количествах он
нетоксичен. Твердый водород плавится при 14 К (–259
°С), а жидкий водород кипит при 20 К (–253 °С). Низкие
температуры плавления и кипения, очень маленький
температурный интервал существования жидкого
водорода (всего 6 °С), а также небольшие значения
молярных теплот плавления (0,117 кДж/моль) и
парообразования (0,903 кДж/моль) говорят о том, что
межмолекулярные связи в водороде очень слабые.
Плотность водорода r(Н 2) = (2 г/моль):(22,4 л/моль)
= 0,0893 г/л. Для сравнения: средняя плотность
воздуха равна 1,29 г/л. То есть водород в 14,5 раза
"легче"воздуха. В воде он практически
нерастворим.
При комнатной температуре водород малоактивен,
но при нагревании реагирует со многими
веществами. В этих реакциях атомы водорода могут
как повышать, так и понижать свою степень
окисления: Н 2 + 2е
– = 2Н –I , Н 2
– 2е
– = 2Н +I .
В первом случае водород является окислителем,
например, в реакциях с натрием или с кальцием: 2Na +
H 2 = 2NaH, (t
) Ca + H 2 = CaH 2 . (t
)
Но более характерны для водорода
восстановительные свойства: O 2 + 2H 2 = 2H 2 O,
(t
)
CuO + H 2 = Cu + H 2 O. (t
)
При нагревании водород окисляется не только
кислородом, но и некоторыми другими неметаллами,
например, фтором, хлором, серой и даже азотом.
В лаборатории водород получают в результате
реакции
Zn + H 2 SO 4 = ZnSO 4 + H 2 .
Вместо цинка можно использовать железо, алюминий и некоторые другие металлы, а вместо серной кислоты – некоторые другие разбавленные кислоты. Образующийся водород собирают в пробирку методом вытеснения воды (см. рис. 10.2 б ) или просто в перевернутую колбу (рис. 10.2 а ).

В промышленности в больших количествах водород получают из природного газа (в основном это метан) при взаимодействии его с парами воды при 800 °С в присутствии никелевого катализатора:
CH 4 + 2H 2 O = 4H 2 +CO 2 (t , Ni)
или обрабатывают при высокой температуре парами воды уголь:
2H 2 O + С = 2H 2 + CO 2 . (t )
Чистый водород получают из воды, разлагая ее электрическим током (подвергая электролизу):
2H 2 O = 2H 2 + O 2 (электролиз).
д) Соединения водорода
Гидриды (бинарные соединения,
содержащие водород) делятся на два основных типа:
а) летучие
(молекулярные) гидриды,
б) солеобразные (ионные) гидриды.
Элементы IVА – VIIA групп и бор образуют
молекулярные гидриды. Из них устойчивы только
гидриды элементов, образующих неметаллы:
B 2 H 6 ;CH 4 ; NH 3 ; H 2 O;
HF
SiH 4 ;PH 3 ; H 2 S; HCl
AsH 3 ; H 2 Se; HBr
H 2 Te; HI
За исключением воды, все эти соединения при
комнатной температуре – газообразные вещества,
отсюда их название – "летучие гидриды" .
Некоторые из элементов, образующих неметаллы,
входят в состав и более сложных гидридов.
Например, углерод образует соединения с общими
формулами C n
H 2n
+2 , C n
H 2n
,
C n
H 2n
–2 и другие, где n
может
быть очень велико (эти соединения изучает
органическая химия).
К ионным гидридам относятся гидриды щелочных,
щелочноземельных элементов и магния. Кристаллы
этих гидридов состоят из анионов Н и катионов металла в высшей
степени окисления Ме
или Ме 2 (в
зависимости от группы системы элементов).
| LiH | |
| NaH | MgH 2 |
| KH | CaH 2 |
| RbH | SrH 2 |
| CsH | BaH 2 |
И ионные, и почти все молекулярные гидриды (кроме
Н 2 О и НF) являются восстановителями, но
ионные гидриды проявляют восстановительные
свойства значительно сильнее, чем молекулярные.
Кроме гидридов, водород входит в состав
гидроксидов и некоторых солей. Со свойствами
этих, более сложных, соединений водорода вы
познакомитесь в следующих главах.
Главными потребителями получаемого в
промышленности водорода являются заводы по
производству аммиака и азотных удобрений, где
аммиак получают непосредственно из азота и
водорода:
N 2 +3H 2 2NH 3 (Р , t , Pt – катализатор).
В больших количествах водород используют для получения метилового спирта (метанола) по реакции 2Н 2 + СО = СН 3 ОН (t , ZnO – катализатор), а также в производстве хлороводорода, который получают непосредственно из хлора и водорода:
H 2 + Cl 2 = 2HCl.
Иногда водород используют в металлургии в качестве восстановителя при получении чистых металлов, например: Fe 2 O 3 + 3H 2 = 2Fe + 3H 2 O.
1.Из
каких частиц состоят ядра а) протия, б) дейтерия,
в) трития?
2.Сравните энергию ионизации атома водорода с
энергией ионизации атомов других элементов. К
какому элементу по этой характеристике водород
ближе всего?
3.Проделайте то же для энергии сродства к
электрону
4.Сравните направление поляризации ковалентной
связи и степень окисления водорода в
соединениях: а) BeH 2 ,CH 4 , NH 3 , H 2 O,
HF; б) CH 4 , SiH 4 ,GeH 4 .
5.Запишите простейшую, молекулярную, структурную
и пространственную формулу водорода. Какая из
них чаще всего используется?
6.Часто говорят: " Водород легче воздуха". Что
под этим подразумевается? В каких случаях это
выражение можно понимать буквально, а в каких
–нет?
7.Составьте структурные формулы гидридов калия и
кальция, а также аммиака, сероводорода и
бромоводорода.
8.Зная молярные теплоты плавления и
парообразования водорода, определите значения
соответствующих удельных величин.
9.Для каждой из четырех реакций, иллюстрирующих
основные химические свойства водорода,
составьте электронный баланс. Отметьте
окислители и восстановители.
10.Определите массу цинка, необходимого для
получения 4,48 л водорода лабораторным способом.
11.Определите массу и объем водорода, который
можно получить из 30 м 3 смеси метана и паров
воды, взятых в объемном отношении 1:2, при выходе 80
%.
12.Составьте уравнения реакций, протекающихпри
взаимодействии водорода а) со фтором, б) с серой.
13.Приведенные ниже схемы реакций иллюстрируют
основные химические свойства ионных гидридов:
а) MH + O 2 MOH (t
); б) MH + Cl 2 MCl + HCl (t
);
в) MH + H 2 O MOH + H 2 ; г) MH + HCl(p) MCl + H 2
Здесь М – это литий, натрий, калий, рубидий или
цезий. Составьте уравнения соответствующих
реакций в случае, если М – натрий.
Проиллюстрируйте уравнениями реакций
химические свойства гидрида кальция.
14.Используя метод электронного баланса,
составьте уравнения следующих реакций,
иллюстрирующих восстановительные свойства
некоторых молекулярных гидридов:
а) HI + Cl 2 HCl + I 2 (t
); б) NH 3 + O 2
H 2 O +
N 2 (t
); в) CH 4 + O 2 H 2 O + CO 2 (t
).
10.2 Кислород
Как и в случае водорода, слово "кислород" является названием и химического элемента, и простого вещества. Кроме простого вещества "кислород" (дикислород) химический элемент кислородобразует еще одно простое вещество, называемое " озон" (трикислород). Это аллотропные модификации кислорода. Вещество кислород состоит из молекул кислорода O 2 , а вещество озон состоит из молекул озона O 3 .
а) Химический элемент кислород
В естественном ряду элементов
порядковый номер кислорода – 8. В системе
элементов кислород находится во втором периоде в
VIA группе.
Кислород – самый распространенный элемент на
Земле. В земной коре каждый второй атом – атом
кислорода, то есть молярная доля кислорода в
атмосфере, гидросфере и литосфереЗемли – около 50
%. Кислород (вещество) – составная часть воздуха.
Объемная доля кислорода в воздухе –21 %. Кислород
(элемент) входит в состав воды, многих минералов,
а также растений и животных. В теле человека
содержится в среднем 43 кг кислорода.
Природный кислород состоит из трех изотопов (16 О,
17 О и 18 О), из которых наиболее
распространен самый легкий изотоп 16 О.
Поэтому атомная масса кислорода близка к 16 Дн
(15,9994 Дн).
б) Атом кислорода
Вам известны следующие характеристики атома кислорода.
Таблица 29. Валентные возможности атома кислорода
Валентное состояние |
Примеры химических веществ |
|||
Al 2 O 3 , Fe 2 O 3 , Cr 2 O 3 * |
||||
–II |
H 2 O, SO 2 , SO 3 ,
CO 2 , SiO 2 , H 2 SO 4 , HNO 2 , HClO 4 ,
COCl 2 , H 2 O 2 |
|||
NaOH, KOH, Ca(OH) 2 , Ba(OH) 2 |
||||
Li 2 O, Na 2 O, MgO, CaO, BaO, FeO, La 2 O 3 |
* Эти оксиды можно рассматривать и как
ионные соединения.
** Атомы кислорода в молекуле не находятся в
данном валентном состоянии; это лишь пример
вещества со степенью окисления атомов кислорода,
равной нулю
Большая энергия ионизации (как у водорода)
исключает образование из атома кислорода
простого катиона. Энергия сродства к электрону
довольно велика (почти в два раза больше, чем у
водорода), что обеспечивает большую склонность
атома кислорода к присоединению электронов и
способность образовывать анионы О 2A . Но
энергия сродства к электрону у атома кислорода
все же меньше, чем у атомов галогенов и даже
других элементов VIA группы. Поэтому анионы
кислорода (оксид-ионы
) существуют только в
соединениях кислорода с элементами, атомы
которых очень легко отдают электроны.
Обобществляя два неспаренных электрона, атом
кислорода может образовать две ковалентные
связи. Две неподеленные пары электронов из-за
невозможности возбуждения могут вступать только
в донорно-акцепторное взаимодействие. Таким
образом, без учета кратности связи и
гибридизации атом кислорода может находиться в
одном из пяти валентных состояний (табл. 29).
Наиболее характерно для атома кислорода
валентное состояние с W
к = 2, то есть
образование двух ковалентных связей за счет двух
неспаренных электронов.
Очень высокая электроотрицательность атома
кислорода (выше – только у фтора) приводит к тому,
что в большинстве своих соединений кислород
имеет степень окисления –II. Существуют вещества,
в которых кислород проявляет и другие значения
степени окисления, некоторые из них приведены в
таблице 29 в качестве примеров, а сравнительная
устойчивость показана на рис. 10.3.

в) Молекула кислорода
Экспериментально установлено, что двухатомная молекула кислорода О 2 содержит два неспаренных электрона. Используя метод валентных связей, такое электронное строение этой молекулы объяснить невозможно. Тем не менее, связь в молекуле кислорода близка по свойствам к ковалентной. Молекула кислорода неполярна. Межатомное расстояние (r o–o = 1,21 A = 121 нм) меньше, чем расстояние между атомами, связанными простой связью. Молярная энергия связи довольно велика и составляет 498 кДж/моль.
г) Кислород (вещество)
При обычных условиях кислород – газ
без цвета и запаха. Твердый кислород плавится при
55 К (–218 °С), а жидкий кислород кипит при 90 К (–183
°С).
Межмолекулярные связи в твердом и жидком
кислороде несколько более прочные, чем в
водороде, о чем свидетельствует больший
температурный интервал существования жидкого
кислорода (36 °С) и большие, чем у водорода,
молярные теплоты плавления (0,446 кДж/моль) и
парообразования (6,83 кДж/моль).
Кислород незначительно растворим в воде: при 0 °С
в 100 объемах воды (жидкой!) растворяется всего 5
объемов кислорода (газа!).
Высокая склонность атомов кислорода к
присоединению электронов и высокая
электроотрицательность приводят к тому, что
кислород проявляет только окислительные
свойства. Эти свойства особенно ярко проявляются
при высокой температуре.
Кислород реагирует со многими металлами: 2Ca + O 2
= 2CaO, 3Fe + 2O 2 = Fe 3 O 4 (t
);
неметаллами: C + O 2 = CO 2, P 4 + 5O 2
= P 4 O 10 ,
и сложными веществами: CH 4 + 2O 2 = CO 2
+ 2H 2 O, 2H 2 S + 3O 2 = 2H 2 O + 2SO 2 .
Чаще всего в результате таких реакций получаются различные оксиды (см. гл. II § 5), но активные щелочные металлы, например натрий, сгорая, превращаются в пероксиды:
2Na + O 2 = Na 2 O 2 .
Структурная формула получившегося
пероксида натрия (Na ) 2 ( O-O ).
Тлеющая лучинка, помещенная в кислород,
вспыхивает. Это удобный и простой способ
обнаружения чистого кислорода.
В промышленности кислород получают из воздуха
путем ректификации (сложной разгонки), а в
лаборатории – подвергая термическому
разложению некоторые кислородсодержащие
соединения, например:
2KMnO 4 = K 2 MnO 4 + MnO 2 + O 2 (200 °С);
2KClO 3 = 2KCl + 3O 2 (150 °С, MnO 2 – катализатор);
2KNO 3 = 2KNO 2 + 3O 2 (400 °С)
и, кроме того, путем каталитического разложения
пероксида водорода при комнатной температуре: 2H 2 O 2
= 2H 2 O + O 2 (MnO 2 –катализатор).
Чистый кислород используют в промышленности для
интенсификации тех процессов, в которых
происходит окисление, и для создания
высокотемпературного пламени. В ракетной
технике в качестве окислителя используется
жидкий кислород.
Огромное значение имеет кислород для
поддержания жизнедеятельности растений,
животных и человека. В обычных условиях человеку
достаточно для дыхания кислорода воздуха. Но в
условиях, когда воздуха не хватает, или он вообще
отсутствует (в самолетах, при водолазных работах,
в космических кораблях и т. п.), для дыхания
готовят специальные газовые смеси, содержащие
кислород. Применяют кислород и в медицине при
заболеваниях, вызывающих затруднение дыхания.
д) Озон и его молекулы
Озон O 3 – вторая аллотропная
модификация кислорода.
Трехатомная молекула озона имеет уголковую
структуру, среднюю между двумя структурами,
отображаемыми следующими формулами:

Озон – темно-синий газ с резким
запахом. Из-за своей сильной окислительной
активности он ядовит. Озон в полтора раза
"тяжелее" кислорода и несколько больше, чем
кислород, растворим в воде.
Озон образуется в атмосфере из кислорода при
грозовых электрических разрядах:
3О 2 = 2О 3 ().
При обычной температуре озон медленно
превращается в кислород, а при нагревании этот
процесс протекает со взрывом.
Озон содержится в так называемом "озоновом
слое" земной атмосферы, предохраняя все живое
на Земле от вредного воздействия солнечного
излучения.
В некоторых городах озон используется вместо
хлора для дезинфекции (обеззараживания) питьевой
воды.
Изобразите структурные формулы следующих
веществ: OF 2 , H 2 O, H 2 O 2 , H 3 PO 4 ,
(H 3 O) 2 SO 4 , BaO, BaO 2 , Ba(OH) 2 .
Назовите эти вещества. Опишите валентные
состояния атомов кислорода в этих соединениях.
Определите валентность и степень окисления
каждого из атомов кислорода.
2.Составьте уравнения реакций сгорания в
кислороде лития, магния, алюминия, кремния,
красного фосфора и селена (атомы селена
окисляются до степени окисления +IV, атомы
остальных элементов – до высшей степени
окисления). К каким классам оксидов относятся
продукты этих реакций?
3.Сколько литров озона можно получить (при
нормальных условиях) а) из 9 л кислорода, б) из 8 г
кислорода?
Вода – самое распространенное в
земной коре вещество. Масса земной воды
оценивается в 10 18 тонн. Вода – основа
гидросферы нашей планеты, кроме того, она
содержится в атмосфере, в виде льда образует
полярные шапки Земли и высокогорные ледники, а
также входит в состав различных горных пород.
Массовая доля воды в человеческом организме
составляет около 70 %.
Вода – единственное вещество, у которого во всех
трех агрегатных состояниях есть свои особые
названия.

Электронное строение молекулы воды
(рис. 10.4 а
) нами было подробно изучено ранее
(см. § 7.10).
Из-за полярности связей О–Н и уголковой формы
молекула воды представляет собой электрический
диполь
.
Для характеристики полярности электрического диполя используется физическая величина, называемая "электрический момент электрического диполя" или просто "дипольный момент" .
В химии дипольный момент измеряют в дебаях: 1 Д = 3,34 . 10 –30 Кл. м
В молекуле воды – две полярные ковалентные связи, то есть два электрических диполя, каждый из которых обладает своим дипольным моментом (и ). Общий дипольный момент молекулы равен векторной сумме этих двух моментов (рис. 10.5):
(Н 2 О) = ![]() ,
,

где q 1 и q 2 – частичные заряды (+) на атомах водорода, а и – межатомные расстояния О – Н в молекуле. Так как q 1 = q 2 = q , а , то
Экспериментально определенные дипольные моменты молекулы воды и некоторых других молекул приведены в таблице.
Таблица 30. Дипольные моменты некоторых полярных молекул
Молекула |
Молекула |
Молекула |
|||
Учитывая дипольный характер молекулы
воды, ее часто схематически изображают следующим
образом:
Чистая вода – бесцветная жидкость без вкуса и
запаха. Некоторые основные физические
характеристики воды приведены в таблице.
Таблица 31. Некоторые физические характеристики воды
Большие значения молярных теплот плавления и парообразования (на порядок больше, чем у водорода и кислорода) свидетельствуют о том, что молекулы воды, как в твердом, так и в жидком веществе, довольно прочно связаны между собой. Эти связи называют "водородными связями" .
ЭЛЕКТРИЧЕСКИЙ
ДИПОЛЬ, ДИПОЛЬНЫЙ МОМЕНТ, ПОЛЯРНОСТЬ СВЯЗИ,
ПОЛЯРНОСТЬ МОЛЕКУЛЫ.
Сколько валентных электронов атома кислорода
принимает участие в образовании связей в
молекуле воды?
2.При перекрывании каких орбиталей образуются
связи между водородом и кислородом в молекуле
воды?
3.Составьте схему образования связей в молекуле
пероксида водорода H 2 O 2 . Что вы можете
сказать о пространственном строении этой
молекулы?
4.Межатомные расстояния в молекулах HF, HCl и HBr
равны, соответственно, 0,92; 1,28 и 1,41. Используя таблицу дипольных
моментов, рассчитайте и сравните между собой
частичные заряды на атомах водорода в этих
молекулах.
5.Межатомные расстояния S – H в молекуле
сероводорода равны 1,34 ,
а угол между связями 92°. Определите значения
частичных зарядов на атомах серы и водорода. Что
вы можете сказать о гибридизации валентных
орбиталей атома серы?
10.4. Водородная связь
Как вы уже знаете, из-за существенной
разницы в электроотрицательности водорода и
кислорода (2,10 и 3,50) у атома водорода в молекуле
воды возникает большой положительный частичный
заряд (q
ч = 0,33 е
), а у атома
кислорода – еще больший отрицательный частичный
заряд (q
ч = –0,66 е
). Вспомним также,
что у атома кислорода есть две неподеленные пары
электронов на sp
3 -гибридных АО. Атом
водорода одной молекулы воды притягивается к
атому кислорода другой молекулы, и, кроме того,
полупустая 1s-АО атома водорода частично
акцептирует пару электронов атома кислорода. В
результате этих взаимодействий между молекулами
возникает особый вид межмолекулярных связей
–водородная связь.
В случае воды образование водородной связи может
быть схематически представлено следующим
образом:

В последней структурной формуле тремя точками (пунктирный штрих, а не электроны!) показана водородная связь.
Водородная связь существует не только
между молекулами воды. Она образуется, если
соблюдаются два условия:
1) в молекуле есть сильно полярная связь Н–Э (Э –
символ атома достаточно электроотрицательного
элемента),
2) в молекуле есть атом Э с большим отрицательным
частичным зарядом и неподеленной парой
электронов.
В качестве элемента Э может быть фтор, кислород и
азот. Существенно слабее водородные связи, если Э
– хлор или сера.
Примеры веществ с водородной связью между
молекулами: фтороводород, твердый или жидкий
аммиак, этиловый спирт и многие другие.
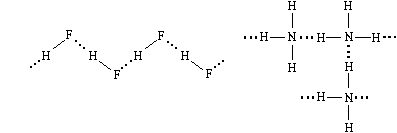
В жидком фтороводороде его молекулы
связаны водородными связями в довольно длинные
цепи, а в жидком и твердом аммиаке образуются
трехмерные сетки.
По прочности водородная связь – промежуточная
между химической связью и остальными видами
межмолекулярных связей. Молярная энергия
водородной связи обычно лежит в пределах от 5 до 50
кДж/моль.
В твердой воде (то есть в кристаллах льда) все
атомы водорода связаны водородными связями с
атомами кислорода, при этом каждый атом
кислорода образует по две водородные связи
(используя обе неподеленные пары электронов).
Такая структура делает лед более " рыхлым"по
сравнению с жидкой водой, где часть водородных
связей оказывается разорванной, и молекулы
получают возможность несколько плотнее "
упаковаться". Эта особенность структуры льда
объясняет, почему, в отличие от большинства
других веществ, вода в твердом состоянии имеет
меньшую плотность, чем в жидком. Максимальной
плотности вода достигает при 4 °С –при этой
температуре рвется достаточно много водородных
связей, а тепловое расширение еще не очень сильно
сказывается на плотности.
Водородные связи имеют очень большое значение в
нашей жизни. Представим себе на минуту, что
водородные связи перестали образовываться. Вот
некоторые последствия:
- вода при комнатной температуре стала бы газообразной, так как ее температура кипения понизилась бы до примерно –80 °С;
- все водоемы стали бы промерзать со дна, так как плотность льда была бы больше плотности жидкой воды;
- перестала бы существовать двойная спираль ДНК и многое другое.
Приведенных примеров достаточно, чтобы понять, что в этом случае природа на нашей планете стала бы совсем иной.
ВОДОРОДНАЯ
СВЯЗЬ, УСЛОВИЯ ЕЕ ОБРАЗОВАНИЯ.
Формула этилового спирта СН 3 –СН 2 –О–Н.
Между какими атомами разных молекул этого
вещества образуются водородные связи? Составьте
структурные формулы, иллюстрирующие их
образование.
2.Водородные связи существуют не только в
индивидуальных веществах, но и в растворах.
Покажите с помощью структурных формул, как
образуются водородные связи в водном растворе а)
аммиака, б) фтороводорода, в) этанола (этилового
спирта).
= 2Н 2 О.
Обе эти реакции протекают в воде постоянно и с
равной скоростью, следовательно, в воде
существует равновесие: 2Н 2 О AН 3 О + ОН .
Это равновесие называется равновесием
автопротолиза
воды.
Прямая реакция этого обратимого
процесса эндотермична, поэтому при нагревании
автопротолиз усиливается, при комнатной же
температуре равновесие сдвинуто влево, то есть
концентрация ионов Н 3 О и ОН
ничтожны. Чему же они равны?
По закону действующих масс
![]()
Но из-за того, что число прореагировавших молекул воды по сравнению с общим числом молекул воды незначительно, можно считать, что концентрация воды при автопротолизе практически не изменяется, и 2 = const Такая низкая концентрация разноименно заряженных ионов в чистой воде объясняет, почему эта жидкость, хоть и плохо, но все же проводит электрический ток.
АВТОПРОТОЛИЗ
ВОДЫ, КОНСТАНТА АВТОПРОТОЛИЗА (ИОННОЕ
ПРОИЗВЕДЕНИЕ) ВОДЫ.
Ионное произведение жидкого аммиака
(температура кипения –33 °С) равно 2·10 –28 .
Составьте уравнение автопротолиза аммиака.
Определите концентрацию ионов аммония в чистом
жидком аммиаке. Электропроводность какого из
веществ больше, воды или жидкого аммиака?
1. Получение водорода и его
горение (восстановительные свойства).
2. Получение кислорода и горение веществ в нем
(окислительные свойства).
§3. Уравнение реакции и как его составить
Взаимодействие водорода
с кислородом
, как это установил еще сэр Генри Кавендиш , приводит к образованию воды.
Давайте на этом простом примере поучимся составлять уравнения химических реакций
.
Что получается из водорода
и кислорода
, мы уже знаем:
Н 2 + О 2 → Н 2 О
Теперь учтем, что атомы химических элементов в химических реакциях не исчезают и не появляются из ничего, не превращаются друг в друга, а соединяются в новых комбинациях , образуя новые молекулы. Значит, в уравнении химической реакции атомов каждого сорта должно быть одинаковое количество до реакции (слева от знака равенства) и после окончания реакции (справа от знака равенства), вот так:
2Н 2 + О 2 = 2Н 2 О
Это и есть уравнение реакции - условная запись протекающей химической реакции с помощью формул веществ и коэффициентов .
Это значит, что в приведенной реакции два моля водорода должны прореагировать с одним молем кислорода , и в результате получится два моля воды .
Взаимодействие водорода с кислородом - совсем не простой процесс. Он приводит к изменению степеней окисления этих элементов. Чтобы подбирать коэффициенты в таких уравнениях, обычно пользуются методом "электронного баланса ".
Когда из водорода и кислорода образуется вода, то это значит, что водород поменял свою степень окисления от 0 до +I , а кислород - от 0 до −II . При этом от атомов водорода к атомам кислорода перешло несколько (n) электронов:
Водород, отдающий электроны, служит здесь восстановителем , а кислород, принимающий электроны - окислителем .
Окислители и восстановители
Посмотрим теперь, как выглядят процессы отдачи и приема электронов по отдельности. Водород , встретившись с "грабителем"-кислородом, теряет все свое достояние - два электрона, и его степень окисления становится равной +I :
Н 2 0 − 2e − = 2Н +I
Получилось уравнение полуреакции окисления водорода.
А бандит-кислород О 2 , отняв последние электроны у несчастного водорода, очень доволен своей новой степенью окисления -II :
O 2 + 4e − = 2O −II
Это уравнение полуреакции восстановления кислорода.
Остается добавить, что и "бандит", и его "жертва" потеряли свою химическую индивидуальность и из простых веществ - газов с двухатомными молекулами Н 2 и О 2 превратились в составные части нового химического вещества - воды Н 2 О .
Дальше будем рассуждать следующим образом: сколько электронов отдал восстановитель бандиту-окислителю, столько тот и получил. Число электронов, отданных восстановителем, должно быть равно числу электронов, принятых окислителем .
Значит, надо уравнять число электронов в первой и второй полуреакциях. В химии принята такая условная форма записи уравнений полуреакций:
2 Н 2 0 − 2e − = 2Н +I |
|
1 O 2 0 + 4e − = 2O −II |
Здесь числа 2 и 1 слева от фигурной скобки - это множители, которые помогут обеспечить равенство числа отданных и принятых электронов. Учтем, что в уравнениях полуреакций отдано 2 электрона, а принято 4. Чтобы уравнять число принятых и отданных электронов, находят наименьшее общее кратное и дополнительные множители. В нашем случае наименьшее общее кратное равно 4. Дополнительные множители будут для водорода равны 2 (4: 2 = 2), а для кислорода - 1 (4: 4 = 1)
Полученные множители и будут служить коэффициентами будущего уравнения реакции:
2H 2 0 + O 2 0 = 2H 2 +I O −II
Водород окисляется не только при встрече с кислородом . Примерно так же на водород действуют и фтор F 2 , галоген и известный "разбойник", и казалось бы, безобидный азот N 2 :
H 2 0 + F 2 0 = 2H +I F −I |
3H 2 0 + N 2 0 = 2N −III H 3 +I |
При этом получается фтороводород HF или аммиак NH 3 .
В обоих соединениях степень окисления водорода становится равной +I , потому что партнеры по молекуле ему достаются "жадные" до чужого электронного добра, с высокой электроотрицательностью - фтор F и азот N . У азота значение электроотрицательности считают равным трем условным единицам, а у фтора вообще самая высокая электроотрицательность среди всех химических элементов - четыре единицы. Так что немудрено им оставить бедняжку-атом водорода без всякого электронного окружения.
Но водород может и восстанавливаться - принимать электроны. Это происходит, если в реакции с ним будут участвовать щелочные металлы или кальций, у которых электроотрицательность меньше, чем у водорода.
Водород – особый элемент, занимающий сразу две ячейки в периодической системе Менделеева. Он располагается в двух группах элементов, обладающих противоположными свойствами, и эта особенность делает его уникальным. Водород является простым веществом и составной частью многих сложных соединений, это органогенный и биогенный элемент. Стоит подробно ознакомиться с основными его особенностями и свойствами.
Водород в периодической системе Менделеева
Главные особенности водорода, указанные в :
- порядковый номер элемента – 1 (протонов и электронов столько же);
- атомная масса составляет 1,00795;
- водород имеет три изотопа, каждый из которых обладает особыми свойствами;
- благодаря содержанию только одного электрона, водород способен проявлять восстановительные и окислительные свойства, а после отдачи электрона водород имеет свободную орбиталь, принимающую участие в составлении химических связей по донорно-акцепторному механизму;
- водород – легкий элемент с небольшой плотностью;
- водород является сильным восстановителем, он открывает группу щелочных металлов в первой группе главной подгруппе;
- когда водород вступает в реакцию с металлами и другими сильными восстановителями, он принимает их электрон и становится окислителем. Такие соединения называются гидридами. По указанному признаку водород условно относится к группе галогенов (в таблице он приводится над фтором в скобках), с которыми он имеет сходство.
Водород как простое вещество
Водород - это газ, молекула которого состоит из двух . Это вещество было открыто в 1766 году британским ученым Генри Кавендишем. Он доказал, что водород является газом, который взрывается при взаимодействии с кислородом. После изучения водорода химики установили, что это вещество является самым легким из всех известных человеку.
Другой ученый, Лавуазье, присвоил элементу имя «гидрогениум», что в переводе с латыни означает «рождающий воду». В 1781 году Генри Кавендиш доказал, что вода является сочетанием кислорода и водорода. Другими словами, вода - это продукт реакции водорода с кислородом. Горючие свойства водорода были известны еще древним ученым: соответствующие записи оставил Парацельс, живший в XVI столетии.
Молекулярный водород - это образующееся естественным путем распространенное в природе газообразное соединение, которое состоит из двух атомов и при поднесении горящей лучинки. Молекула водорода может распадаться на атомы, превращающиеся в ядра гелия, так как они способны участвовать в ядерных реакциях. Такие процессы регулярно протекают в космосе и на Солнце.
Водород и его физические свойства
Водород имеет такие физические параметры:
- кипит при температуре -252,76 °C;
- плавится при температуре -259,14 °C; *в указанных температурный пределах водород - это не имеющая запаха бесцветная жидкость;
- в воде водород слабо растворяется;
- водород теоретически может перейти в металлическое состояние при обеспечении особых условий (низких температур и высокого давления);
- чистый водород - взрывоопасное и горючее вещество;
- водород способен диффундировать сквозь толщу металлов, поэтому хорошо в них растворяется;
- водород легче воздуха в 14,5 раз;
- при высоком давлении можно получить снегообразные кристаллы твердого водорода.
Химические свойства водорода

Лабораторные способы:
- взаимодействие разбавленных кислот с активными металлами и металлами средней активности;
- гидролиз гидридов металлов;
- реакция с водой щелочных и щелочноземельных металлов.
Соединения водорода:
Галогенводороды; летучие водородные соединения неметаллов; гидриды; гидроксиды; гидроксид водорода (вода); пероксид водорода; органические соединения (белки, жиры, углеводороды, витамины, липиды, эфирные масла, гормоны). Нажмите , чтобы увидеть безопасные эксперименты на изучение свойств белков, жиров и углеводов.
Чтобы собрать образующийся водород, нужно держать пробирку перевернутой вверх дном. Водород нельзя собрать, как углекислый газ, ведь он намного легче воздуха. Водород быстро улетучивается, а при смешении с воздухом (или при большом скоплении) взрывается. Поэтому необходимо переворачивать пробирку. Сразу после заполнения пробирка закрывается резиновой пробкой.
Чтобы проверить чистоту водорода, нужно поднести зажженную спичку к горлышку пробирки. Если произойдет глухой и тихий хлопок - газ чистый, а примеси воздуха минимальные. Если хлопок громкий и свистящий - газ в пробирке грязный, в нем присутствует большая доля посторонних компонентов.
Внимание! Не пытайтесь повторить эти опыты самостоятельно!
Водород H — самый распространённый элемент во Вселенной (около 75 % по массе), на Земле — девятый по распространенности. Наиболее важным природным соединением водорода является вода.
Водород занимает первое место в периодической системе (Z = 1). Он имеет простейшее строение атома: ядро атома – 1 протон, окружено электронным облаком, состоящим из 1 электрона.
В одних условиях водород проявляет металлические свойства (отдает электрон), в других - неметаллические (принимает электрон).
В природе встречаются изотопы водорода: 1Н — протий (ядро состоит из одного протона), 2Н — дейтерий (D — ядро состоит из одного протона и одного нейтрона), 3Н — тритий (Т — ядро состоит из одного протона и двух нейтронов).
Простое вещество водород
Молекула водорода состоит из двух атомов, связанных между собой ковалентной неполярной связью.
Физические свойства.
Водород — бесцветный нетоксичный газ без запаха и вкуса. Молекула водорода не полярна. Поэтому силы межмолекулярного взаимодействия в газообразном водороде малы. Это проявляется в низких температурах кипения (-252,6 0С) и плавления (-259,2 0С).
Водород легче воздуха, D (по воздуху) = 0,069; незначительно растворяется в воде (в 100 объемах H2O растворяется 2 объема H2). Поэтому водород при его получении в лаборатории можно собирать методами вытеснения воздуха или воды.

Получение водорода
В лаборатории :
1.Действие разбавленных кислот на металлы:
Zn +2HCl → ZnCl 2 +H 2
2.Взаимодействие щелочных и щ-з металлов с водой:
Ca +2H 2 O → Ca(OH) 2 +H 2
3.Гидролиз гидридов: гидриды металлов легко разлагаются водой с образованием соответствующей щелочи и водорода:
NaH +H 2 O → NaOH +H 2
СаH 2 + 2Н 2 О = Са(ОН) 2 + 2Н 2
4.Действие щелочей на цинк или алюминий или кремний:
2Al +2NaOH +6H 2 O → 2Na +3H 2
Zn +2KOH +2H 2 O → K 2 +H 2
Si + 2NaOH + H 2 O → Na 2 SiO 3 + 2H 2
5. Электролиз воды. Для увеличения электрической проводимости воды к ней добавляют электролит, например NаОН, Н 2 SO 4 или Na 2 SO 4 . На катоде образуется 2 объема водорода, на аноде - 1 объем кислорода.
2H 2 O → 2H 2 +О 2
Промышленное получение водорода
1. Конверсия метана с водяным паром, Ni 800 °С (самый дешевый):
CH 4 + H 2 O → CO + 3 H 2
CO + H 2 O → CO 2 + H 2
В сумме:
CH 4 + 2 H 2 O → 4 H 2 + CO 2
2. Пары воды через раскаленный кокс при 1000 о С:
С + H 2 O → CO + H 2
CO +H 2 O → CO 2 + H 2
Образующийся оксид углерода (IV) поглощается водой, этим способом получают 50 % промышленного водорода.
3. Нагреванием метана до 350°С в присутствии железного или никелевого катализатора:
СH 4 → С + 2Н 2
4. Электролизом водных растворов KCl или NaCl, как побочный продукт:
2Н 2 О + 2NaCl→ Cl 2 + H 2 + 2NaOH
Химические свойства водорода
- В соединениях водород всегда одновалентен. Для него характерна степень окисления +1, но в гидридах металлов она равна -1.
- Молекула водорода состоит из двух атомов. Возникновение связи между ними объясняется образованием обобщенной пары электронов Н:Н или Н 2
- Благодаря этому обобщению электронов молекула Н 2 более энергетически устойчива, чем его отдельные атомы. Чтобы разорвать в 1 моль водорода молекулы на атомы, необходимо затратить энергию 436 кДж: Н 2 = 2Н, ∆H° = 436 кДж/моль
- Этим объясняется сравнительно небольшая активность молекулярного водорода при обычной температуре.
- Со многими неметаллами водород образует газообразные соединения типа RН 4 , RН 3 , RН 2 , RН.
1) С галогенами образует галогеноводороды:
Н 2 + Cl 2 → 2НСl.
При этом с фтором — взрывается, с хлором и бромом реагирует лишь при освещении или нагревании, а с йодом только при нагревании.
2) С кислородом:
2Н 2 + О 2 → 2Н 2 О
с выделением тепла. При обычных температурах реакция протекает медленно, выше 550°С — со взрывом. Смесь 2 объемов Н 2 и 1 объема О 2 называется гремучим газом.
3) При нагревании энергично реагирует с серойь(значительно труднее с селеном и теллуром):
Н 2 + S → H 2 S (сероводород),
4) С азотом с образованием аммиака лишь на катализаторе и при повышенных температурах и давлениях:
ЗН 2 + N 2 → 2NН 3
5) С углеродом при высоких температурах:
2Н 2 + С → СН 4 (метан)
6) С щелочными и щелочноземельными металлами образует гидриды (водород – окислитель):
Н 2 + 2Li → 2LiH
в гидридах металлов ион водорода заряжен отрицательно (степень окисления -1), то есть гидрид Na + H — построен подобно хлориду Na + Cl —
Со сложными веществами:
7) С оксидами металлов (используется для восстановления металлов):
CuO + H 2 → Cu + H 2 O
Fe 3 O 4 + 4H 2 → 3Fe + 4Н 2 О
8) с оксидом углерода (II):
CO + 2H 2 → CH 3 OH
Синтез — газ (смесь водорода и угарного газа) имеет важное практическое значение, тк в зависимости от температуры, давления и катализатора образуются различные органические соединения, например НСНО, СН 3 ОН и другие.
9)Ненасыщенные углеводороды реагируют с водородом, переходя в насыщенные:
С n Н 2n + Н 2 → С n Н 2n+2 .










